ECMO Kanülierung: Hilfe bei der Punktion durch Ultraschall
Oder: ich denke, ohne Ultraschall solltest du nicht punktieren
Die Kanülierung fängt mit der Punktion an. Sie ist das Nadelöhr der gesamten Prozedur. Der Erfolg entscheidet über den Verlauf der folgenden invasiven Schritte und kann für Patient*innen lebensentscheidend sein.
Im Podcast spreche ich mit dem leitenden Perfusionisten Dr. Dirk Buchwald über Gefahren und mögliche Probleme bei der ECMO-Kanülierung. Der Schwerpunkt liegt auf dem Einsatz der Sonografie in dieser Prozedur. Zusätzlich werden Indikationen und das Funktionsprinzip einer ECMO erläutert.
Inhaltsverzeichnis
Podcast - ECMO Kanülierung mit Dr. Dirk Buchwald
Begleitmaterial zum Podcast ECMO Kanülierung (S1E13)
Ergänzend zum gesprochenen Wort findest du hier Fotos, Zeichnungen und Ultraschallaufnahmen.
Extrakorparale Membranoxygernierung: ECMO
Was kann die ECMO bieten und was wird dafür benötig?
ECMO, die Abkürzung für Extracorporeal Membrane Oxygenation, ist ein Organunterstützungsverfahren für den Akuteinsatz. Es ermöglicht die temporäre Übernahme der Herz- und Lungenfunktion, um die erkrankten Organe zu entlasten oder Zeit für weitere Diagnostik oder Therapien zu gewinnen.
Mit einer ECMO können im Wesentlichen 4 Effekte erzielt werden:
- Oxygenierung des Blutes durch vollständige Aufsättigung des Hämoglobins
- Dekarboxylierung
- Aufrechterhaltung des Blutdrucks, unabhängig von der Herzfunktion
- Temperierung des Blutes
Die jeweiligen Effekte dabei sind von der Art der Kanülierung abhängig, d.h. wie die ECMO an die Patienten*innen angeschlossen wird.
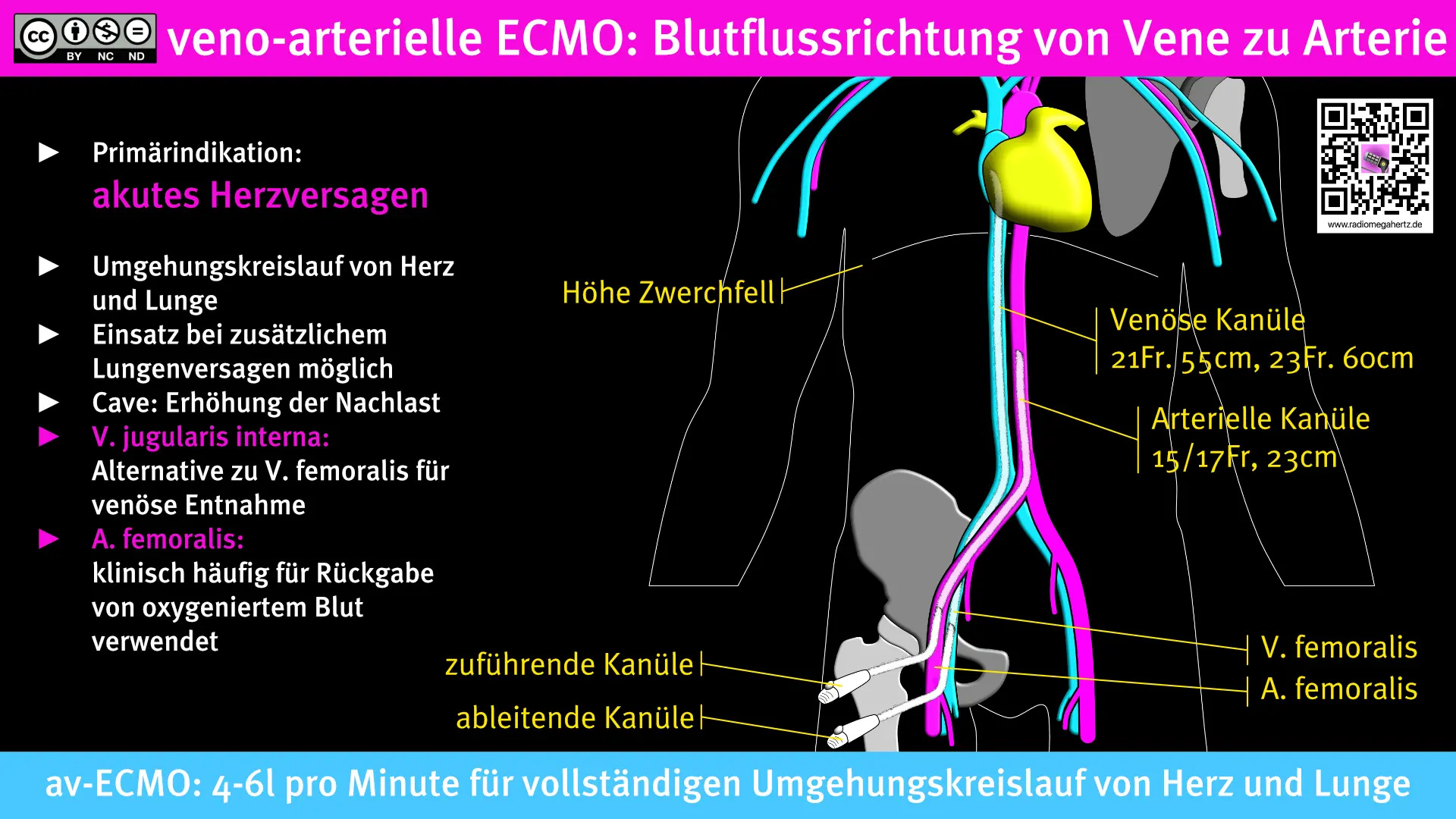
V-A ECMO
Die V-A ECMO ist indiziert bei verschiedenen Formen des akuten Herzversagens. Hierzu zählen zum Beispiel der komplikative akute Myocardinfarkt, maligne Rhythmusstörungen (Kammerflimmern) oder schwere Myocarditiden.
Für den Anschluß der ECMO an das Gefäßsystem werden eine großlumige Vene sowie eine Arterie benötigt. Die Blutflußrichtung ist von venös nach arteriell. Das aktiv über eine (Zentrifugal-) Pumpe abgesaugte Blut wird durch den Oxygenator (=“künstliche Lunge“) geleitet, in dem der Gasaustausch stattfindet.
Das Blut ist danach voll oxygeniert, normokapnisch und in der Regel normotherm. Über einen geeigneten Zugang wird das Blut dann in das arterielle Gefäßsystem gepumpt, wo es den Blutdruck erhöht und eine ausreichende Organperfusion gewährleistet, unabhängig von der Herz- und Lungenfunktion.
V-V ECMO
Liegt ein isoliertes Lungenversagen bei erhaltener Herzfunktion vor, kann die ECMO selektiv die Lungen unterstützen. Der Anschluß erfolgt hierbei über zwei venöse Gefäße (V-V ECMO). Über eine ableitende Kanüle wird das Blut wieder dem Oxygenator zugeführt und danach zurück in ein ebenfalls venöses Gefäß gepumpt. Die Blutflußrichtung ist von venös nach venös. Auf diese Weise werden der Sauerstoffgehalt des stark entsättigten Blutes und das Sauerstoffangebot (DO2) für den Körper insgesamt erhöht. Gleichzeitig kann die mechanische Beatmung am Respirator deeskaliert werden im Richtung einer lungenprotektiven Beatmung. Bei der V-V ECMO findet keine (direkte) Herzentlastung statt, eine ausreichende Herzfunktion ist unerlässlich.
Punktionsset für ECMO Kanülen
Um die großlumigen ECMO-Kanülen nach intravasal einbringen zu können, müssen Haut und Gefäß durch aufsteigende Dilatatorengrößen aufgedehnt werden. Übliche Sets beinhalten verschiedene Dilatatoren bis 24 Fr., eine Punktionskanüle sowie einen Führungsdraht von 180 cm Länge. Dieser ist erforderlich, um die bis zu 60 cm langen Perfusionskanülen sicher und in loco typico im Gefäß positionieren zu können. Die Punktionskanülen sind nicht ultraschalloptimiert, daher sollte gegebenenfalls auf ein anderes Modell zurückgegriffen werden.
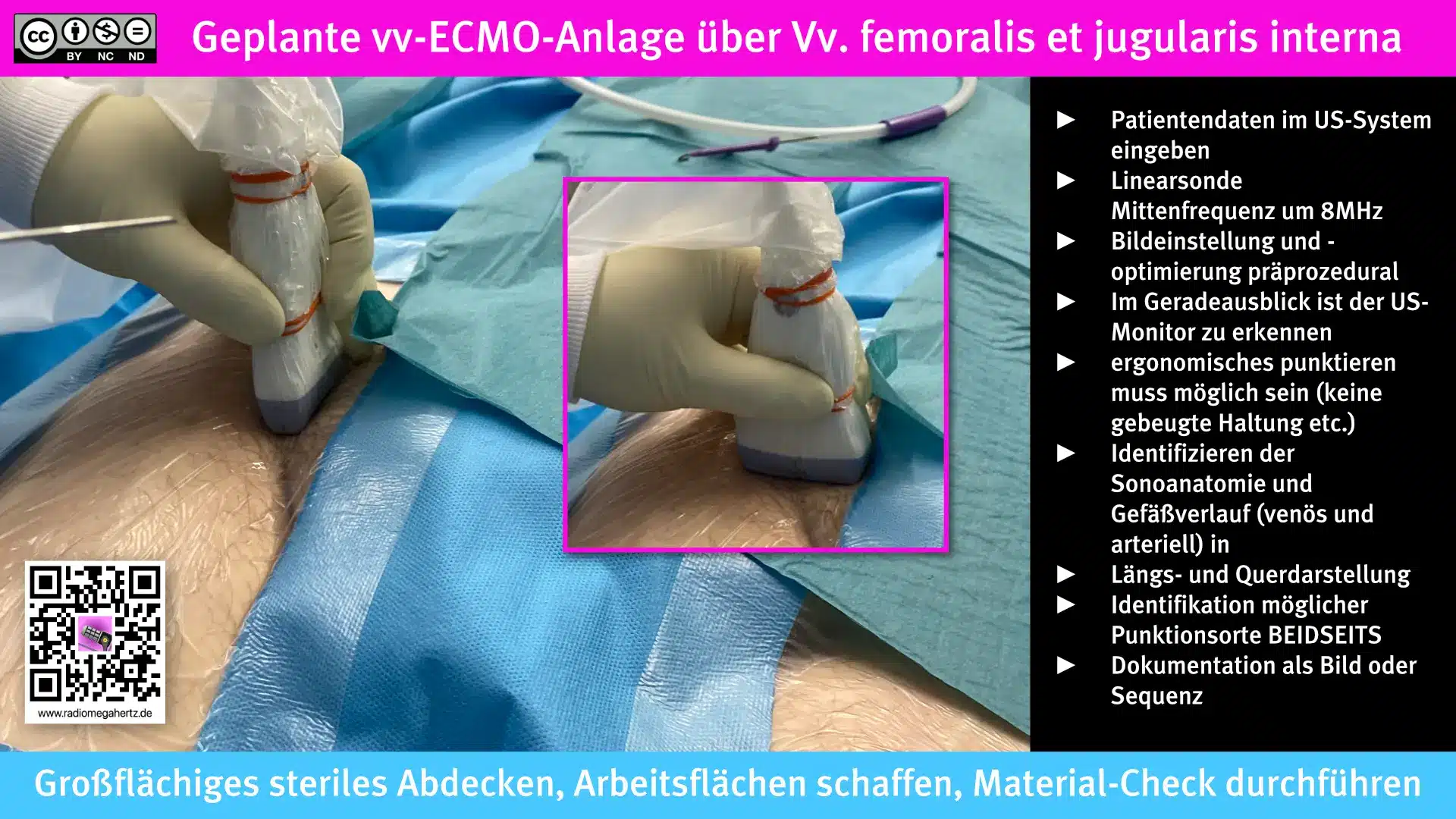
Vorbereitungen, Aufbau, Ultraschalluntersuchung
Mit einer vorausgehenden Sonografie der femoralen Gefäße kannst du sicherstellen, ob die Gefäße überhaupt und wenn ja, wo punktiert werden können. Führe die Ultraschalluntersuchung auf beiden Seiten durch.
Sonografie und Punktion in der Leiste
Sonografie der A. femoralis mit ausgeprägten Plaques und Einengung der Arterie
Nach anatomischer Nomenklatur heißt die A. femoralis einfach nur A. femoralis und wird nicht weiter unterteilt. Klinisch kann zwischen der A. femoralis communis und A. femoralis superficialis nach Abgang der A. profunda femoris gesprochen werden.
Du solltest immer versuchen, die A. femoralis communis für die großlumige ECMO-Kanüle zu punktieren. Die Wahrscheinlichkeit für eine gefährliche Gefäßokklusion durch die ECMO-Kanüle wird hierdurch reduziert. Die A. femoralis communis ist als Fortführung der A. iliaca externa bis zum Abgang der A. profunda femoris nur wenige Zentimeter lang.
Du solltest dir daher die Zeit nehmen, die Gefäßverläufe und die umgebende Sonoanatomie eindeutig bestimmen zu können.
Das klingt zunächst zeitintensiv und steht auf den ersten Blick konträr zum Zeitdruck unter Notfallbedingungen, ist es aber nicht, solange du mit der Sonoantomie und den Sondenmanövern vertraut bist.
Unumstritten bleibt aber die Herausforderung, unter Reanimationen mit Herzdruckmassage sonografieren oder punktieren zu müssen, da Bewegungen die Sonden- und Kanülenführung signifikant erschweren.
Deep-Dive zur Anatomie in der Leistenregion zur Kanülierung
Für ein ausführliches Verständnis zur Anatomie der femoralen Region gibt es einen Videocast und Blogbeitrag mit anatomischen Schnitten auf Radiomegahertz.
Sonografische Bestimmung des Arterienabschnittes für die Punktion und Kanülierung
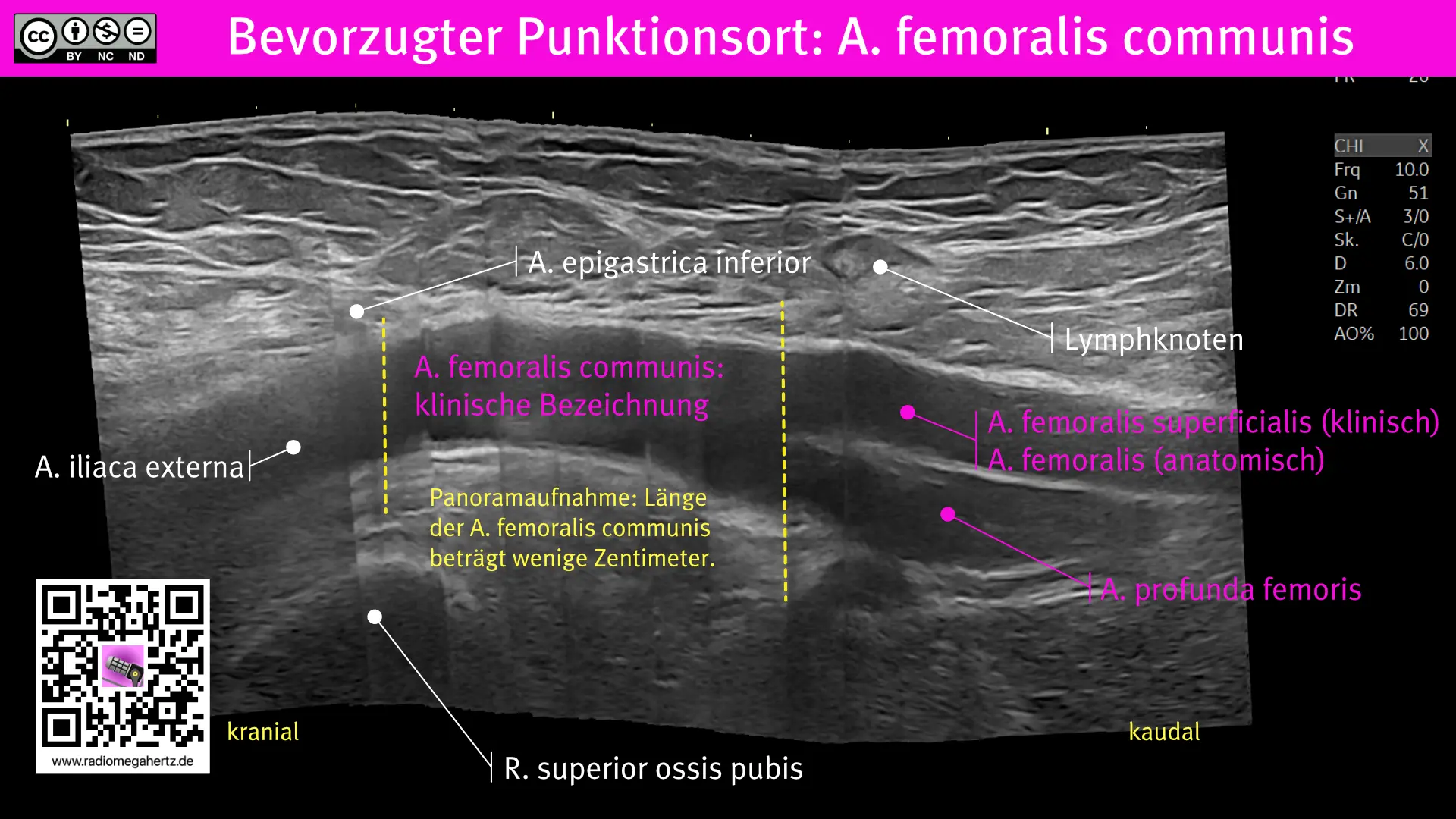
Punktionsziel ist die A. femoralis communis (Beispiel V-A ECMO). Der Abschnitt liegt zwischen A. iliaca externa und Abgang der A. profuda femoris.
Die folgende Abbildung der Arterie ist mit einer Panaromafunktion erstellt: mehrere Ultraschallaufnahmen werden zusammengeführt, so ist der Gefäßverlauf eindeutig zu erkennen. Die A. iliaca exsterna steigt im Verlauf nach kranial vom Ramus superior des ossis pubis nach dorsal ab, dieser anatomische Verlauf sollte beim Vorschieben der steifen Dilatatioren oder der metallarmierten ECMO-Kanüle berücksichtigt werden.
Radiologisch orientieren sich Interventionalist*innen am Femurkopf zur Punktion der A. femoralis communis, doch sonografisch geht ohne ohne Strahlenbelastung und präziser.
Plane sonografisch den Punktionsweg, indem du bei schwerer Arteriosklerose der A. femoralis eine Region mit keiner oder geringer Plaque-Bildung auswählt. Diesen sonografischen Vorteil gegenüber der Landmarkentechnik erhälst du jedoch nur, wenn deine Fertig– und Fähigkeiten zur Kanülenführungen entsprechend ausgebildet sind 😉
Messung des Arteriendurchmessers VOR Kanülierung
Vor jeder ECMO-Kanülierung wird entschieden: passt die Kanülengröße zum benötigten Blutfluss und kann das Zielgefäß kanüliert werden. Während Körpergröße, Blutvolumen und benötigte Flussrate in Abhängigkeit vom Kanülendurchmesser zu berechnen sind, ist der Gefäßdurchmesser zunächst eine unbekannte Grösse.
Zum Beispiel wird A. femoralis-Durchmesser eines erwachsenen Mannes je nach Quelle zwischen 5-11mm angegeben. Die nächste Abbildung zeigt wie einfach mit einer Standard–Linearsonde (10Mhz) der Durchmesser bestimmt werden kann.
Die scharfe Reflexion an der Tunica intima, schallkopfnah UND schallkopffern, ist ein Gütekriterium für die mittige Gefäßdarstellung im Längsschnitt, was der Mitte des Schallvolumens entspricht.

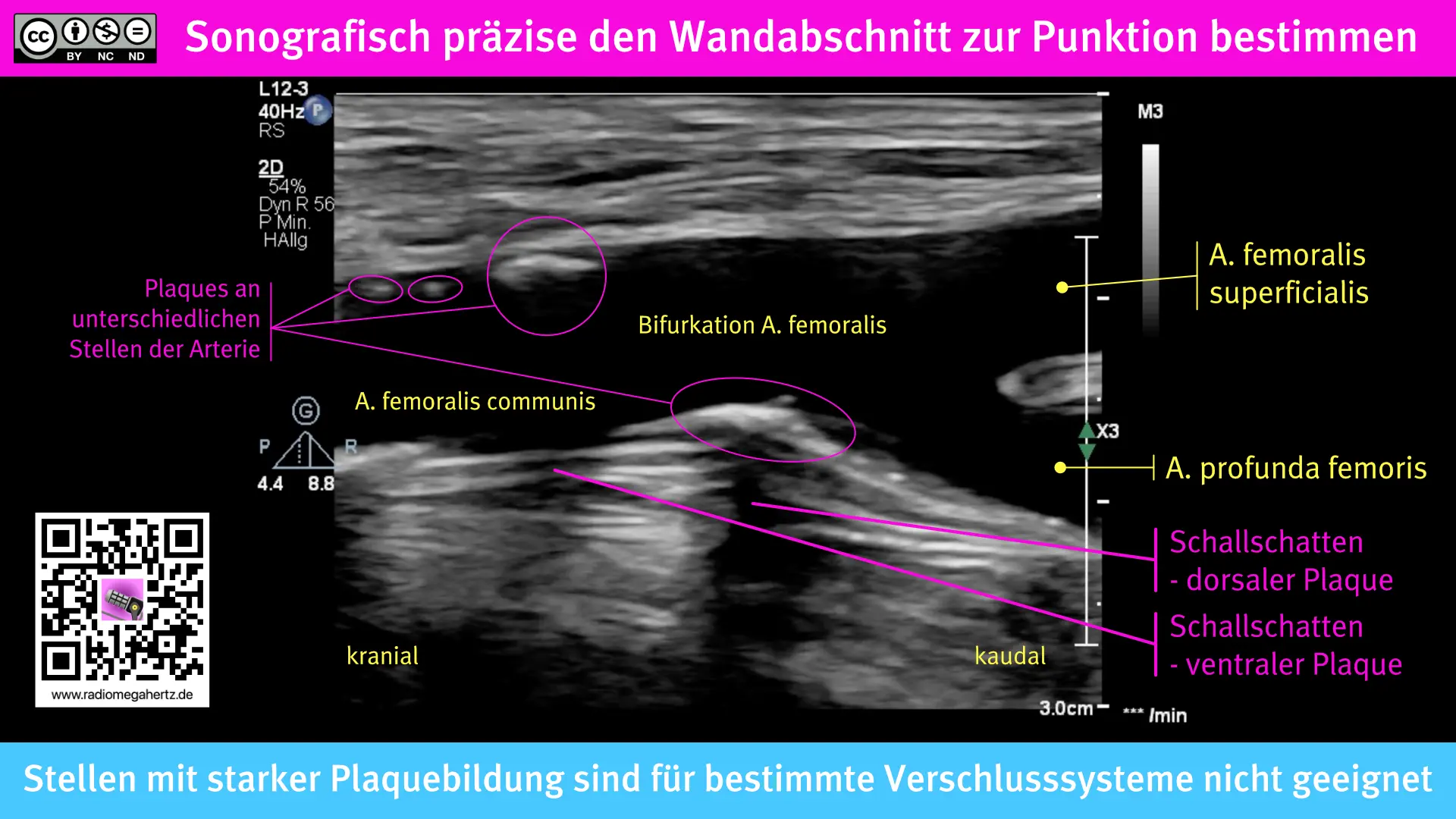
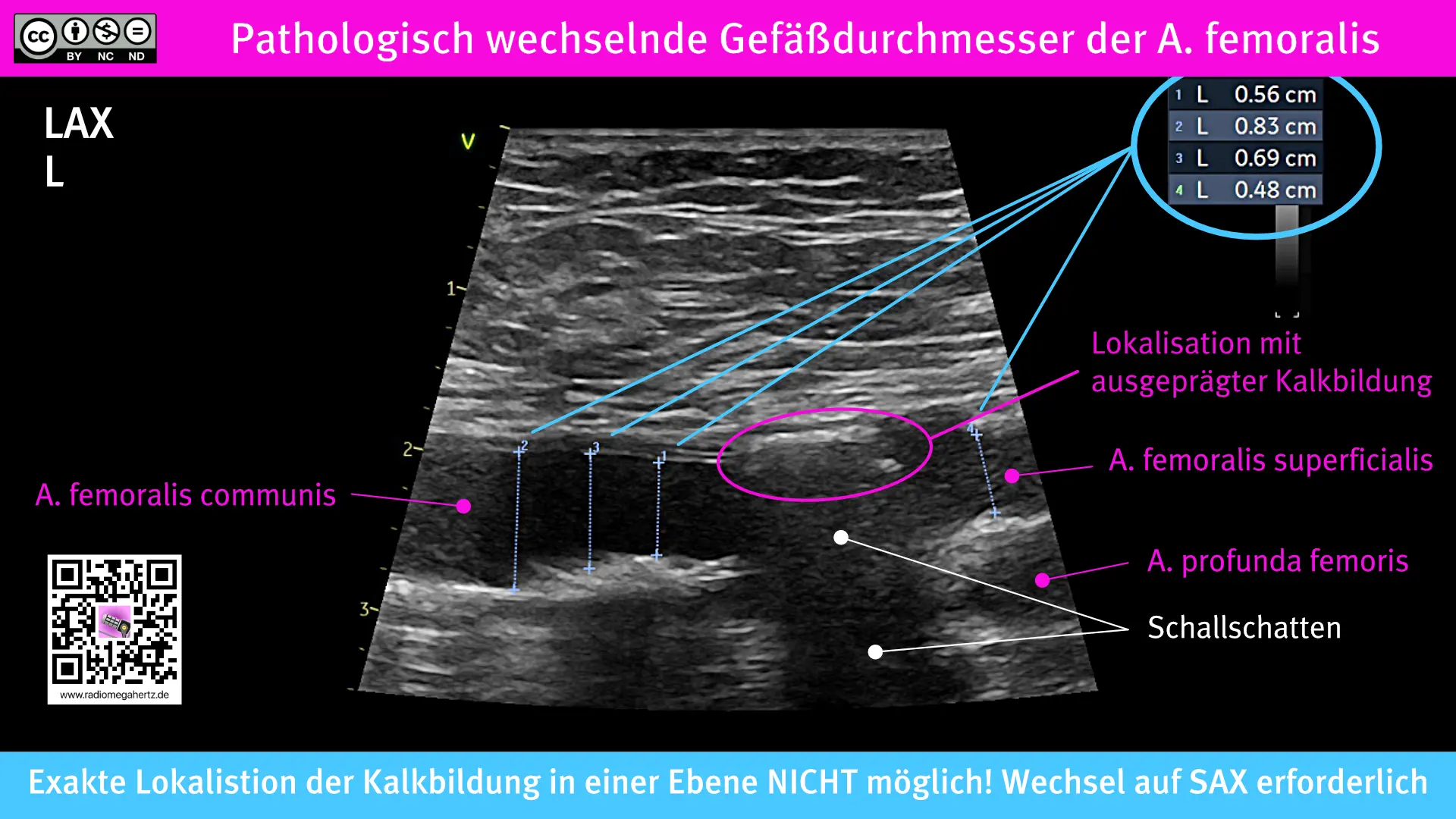
Bei pathologisch veränderten Gefäßen wie in der nächsten Abbildung dargestellt, kann es schwierig sein, den besten Ort zur Kanülierung bestimmen zu können.
Du siehst vier verschiedene Messungen an vier verschiedenen Orten. Der Durchmesser wechselt von von 4,8 bis 8,3mm. Einen Ort mit besonders ausgeprägter Kalkbildung ist markiert.
Vergleich die obige Ultraschallaufnahme mit der Folgenden: der Schallkopf wurde um einige Millimeter nach medial verschoben, der Befund wird deutlicher erkennbar.
Um aber exakt bestimmen zu können, ob die Verminderung des Arterienlumens zirkulär oder nur einen Bereich der Arterienwand betrifft, ist der Wechsel von der Längs– auf die Querdarstellung hilfreich (übernächste Abbildung).
Die Stelle mit der stärksten Einengung des Arterienlumens wurde in diesem Fall durch die Querdarstellung und ein Gleitmanöver bestimmt. Darum: Gefäße längs UND quer darstellen.
Punktionstechnik: in-plane oder out-of-plane?
Welche Technik der Punktion die beste ist, quer oder längs zur Schallebene, wird unter Ärzt*innen mit Liebe und innig diskutiert. Nüchtern und objektiv betrachtet gibt es keine Evidenz für die eine oder die andere Punktionstechnik. Persönliche Meinungen basieren anscheinend auf der Erfahrung die die Person gesammelt hat. Nicht selten wird eine Technik gegenüber der anderen besser beherrscht und daraus wird eine Meinung über die vermeintlich bessere abgeleitet.
Recht haben diejenigen, die die Kanülenspitze visuell führen und parallel die individuelle Anatomie berücksichtigen können. Sie kennen die Ultraschallphysik und können daher ein Sonogramm anatomisch korrekt interpretieren.
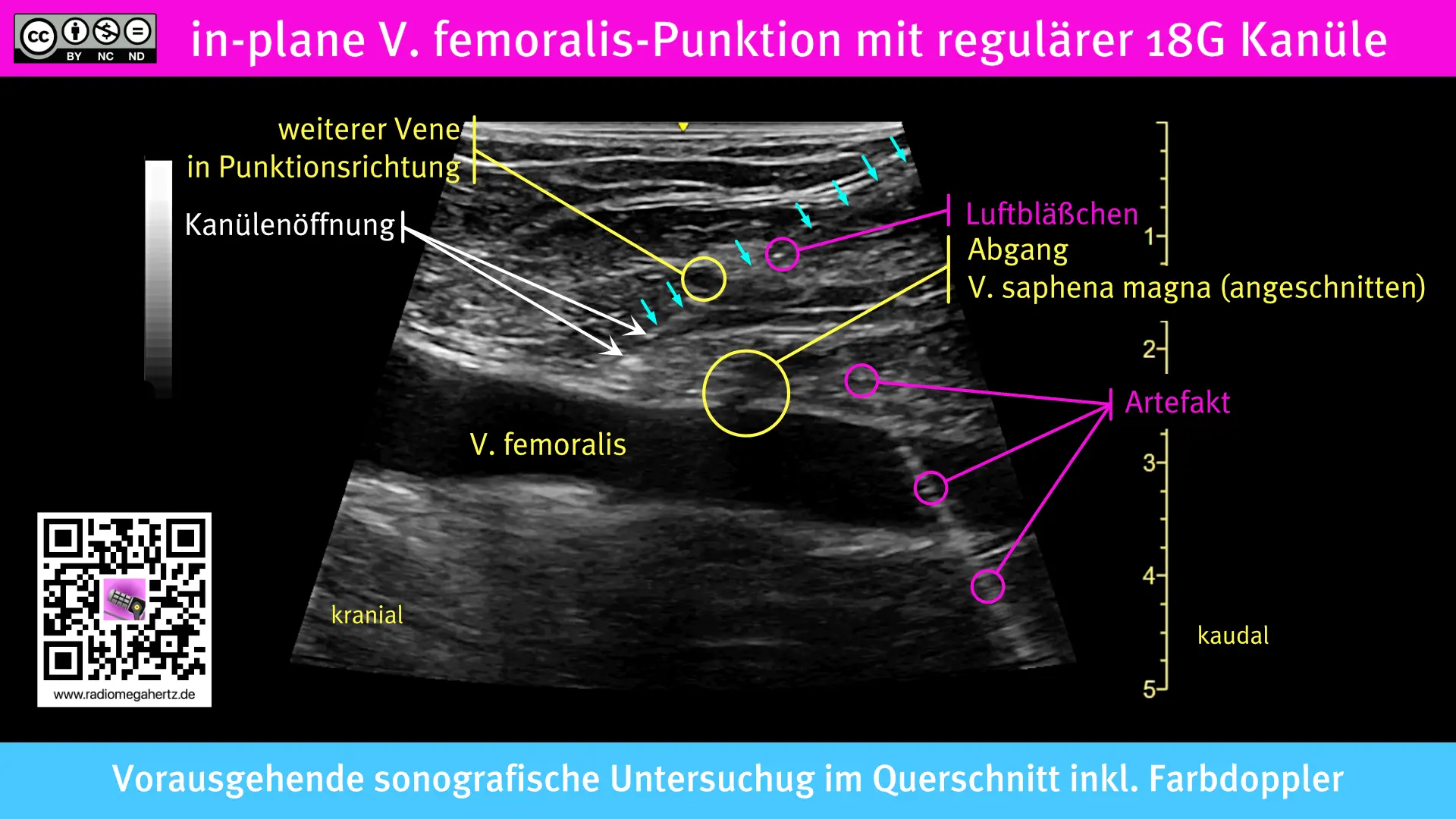
Die folgende Ultraschallaufnahmen zeigt eine V. femoralis Punktion in in-plane-Technik (IP) für die folgende venöse ECMO-Kanülierung. Es wurde eine nicht-ultraschalloptimierte Punktionskanüle verwendet. Die Kanülenspitze ist bei korrektem Alignment gegenüber dem Kanülenschaft aber gut zu erkennen.
Ein möglicher Vorteil der IP-Technik kann sein, dass die punktierende Person gezwungen ist, einen flachen Punktionswinkel einhalten zu müssen, der für das folgende Einführen von Dilatatoren und ECMO-Kanüle vorteilhaft ist.
Weitere Ultraschallaufnahmen der V. femoralis und der Punktion
Auch andere Fachdisziplinen punktieren die femoralen Gefäße. Die Punktionstechniken sind analog zur Anlage von ECMO-Kanülen. Zum Blogbeitrag über eine kardiologische Intervention, bei der in die V. femoralis zwei Schleusen platziert werden.
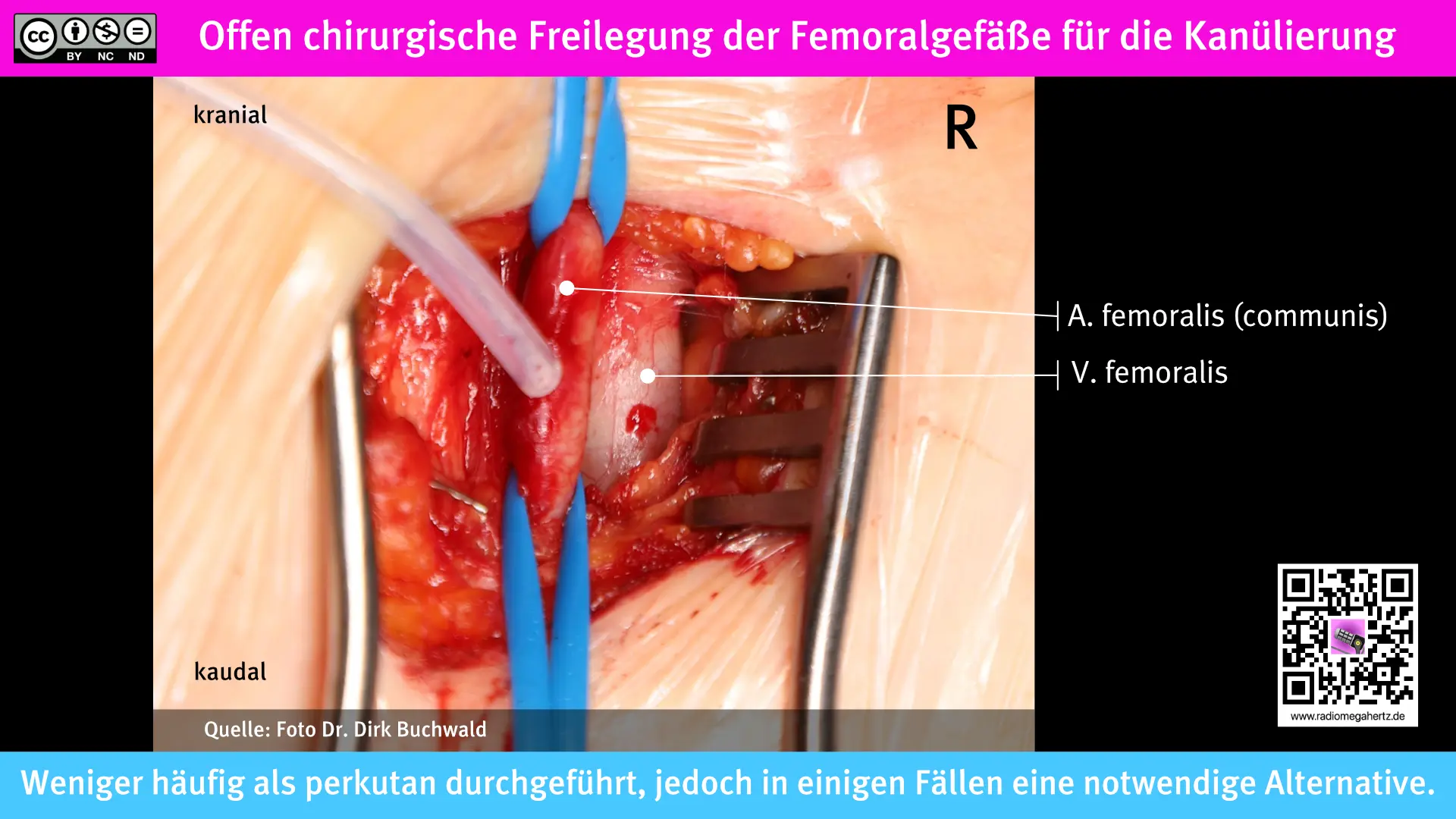
Offen chirurgische gegenüber perkutaner Kanülierung
Neben der perkutanen Kanülierung können die Gefäße auch offen chirurgisch freigelegt und folgend kanüliert werden. Nachteilig könnte im Notfall sein, dass Ärzte*innen einer weiteren Fachdisziplin anwesend sein müssen. Allerdings kann ein operatives Vorgehen auch die einzige Wahl sein, wenn eine perkutane Punktion nicht möglich ist. Alternativ zu den Femoralgefäßen ist auch die chirurgische Kanülierung der A. axillaris möglich, die hierfür operativ freigelegt wird.
Diese Vorgehensweise hat den Vorteil einer antegraden systemischen Perfusion, da das Blut im Systemkreislauf die physiologisch fast normale Flußrichtung aufweist, im Gegensatz zur transfemoralen Perfusion, bei der eine Blutflußrichtung von distal nach proximal in der Aorta stattfindet. Am Ende des Beitrages findet du einen Link zur Studie von Wang et al. zur perkutanen gegenüber der chirurgischen Femoral-Kanülierung (Diskussion lesen). Schwerpunkt auf Radiomegahertz ist die perkutane, ultraschallgestützte Kanülierung.
Cheney und McCabe berichten in einem Review (Referenz am Ende) über die perkutane A. axillaris-Kanülierung: Um Blutungen bei der De-Kanülierung zu vermeiden, kann die A. axillaris manuell gegen die erste Rippe gedrückt werden. Anatomisch ist das nachvollziehbar, Voraussetzung ist aber, dass die Kanüle an adäquater Stelle eingesetzt wurde. Die A. axillaris Kanülierung ist offen chirurgisch und sonographisch möglich, für die Explantation ist aus unserer Sicht die chirurgische Vorgehensweise empfehlenswert.
Wichtige Schritte bei der Kanülenanlage nach erfolgreicher Punktion...
... bei denen die Sonographie mal keine Hilfe ist!
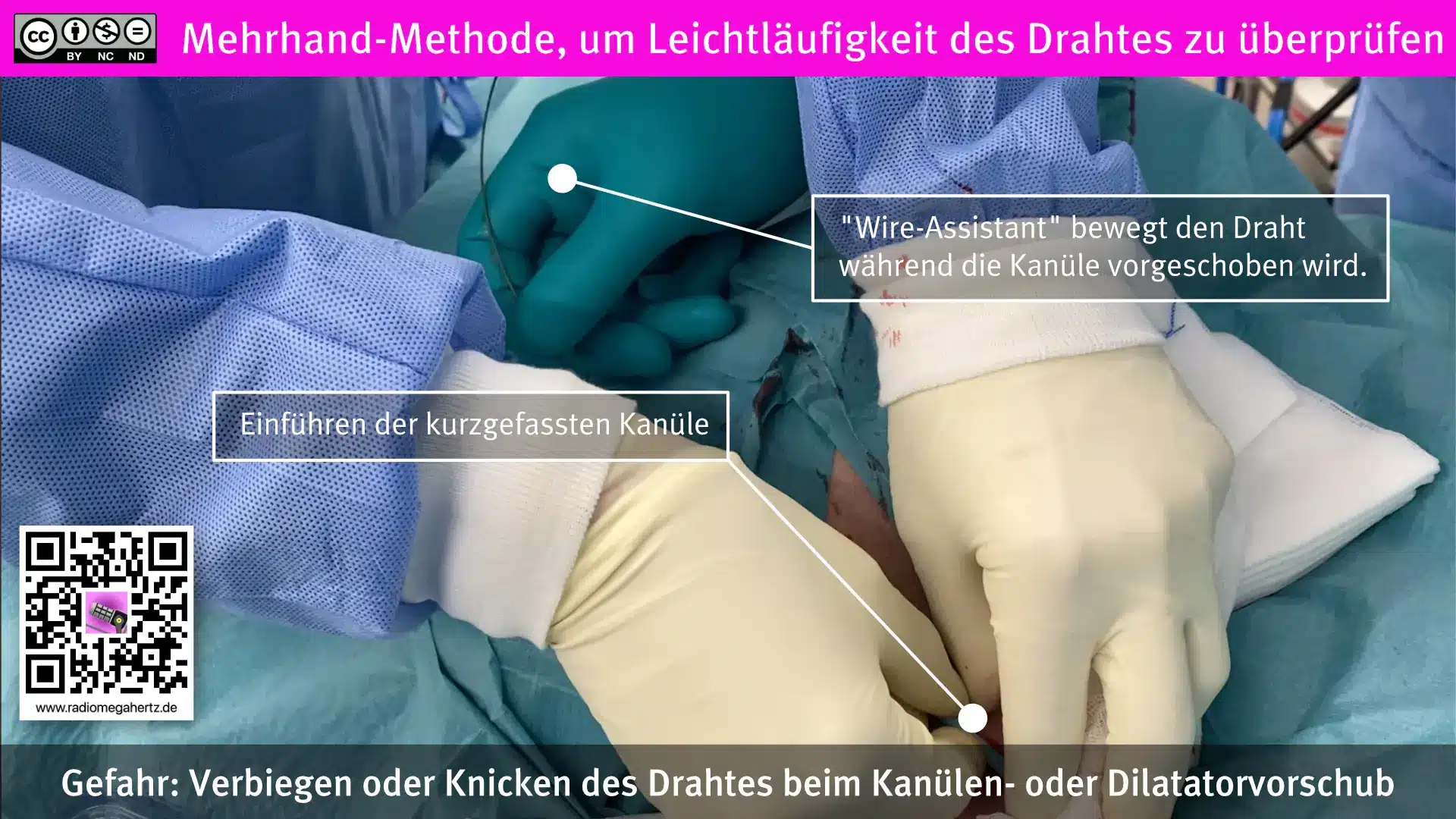
Alle uns bekannten ECMO-Kanülen weisen eine Stufe zwischen dem Mandrin und der eigentlichen metallarmierten Kanüle auf. Beim Einführen der Kanüle muss eine nicht unerhebliche Kraft aufgewendet werden, um zunächst die Hautschicht und dann den Übergang in das Gefäß zu überwinden. Dieser Schritt birgt ein erhöhtes Risiko hinsichtlich Gefäßverletzungen.
Während eine Person die ECMO-Kanüle über den Führungsdraht einbringt, hilft eine zweite Person („Wire assistant“), den Draht zu führen und gleichzeitig die Leichtläufigkeit zu fühlen. Stockt der Draht oder lässt er sich während des Vorschiebens der Kanüle nicht widerstandlos vor– und zurückbewegen, ist dieses ein Indiz für ein Abknicken oder eine Fehllage. Die Kanüle sollte in diesem Fall keinesfalls weiter vorgeschoben werden. Zwei abschreckende Fallbeispiele fehlliegender Kanülen findest du weiter unten im Blogbeitrag.
Ultraschall in der ECMO-Therapie jenseits der Punktion
Transöphageale Echokardiografie
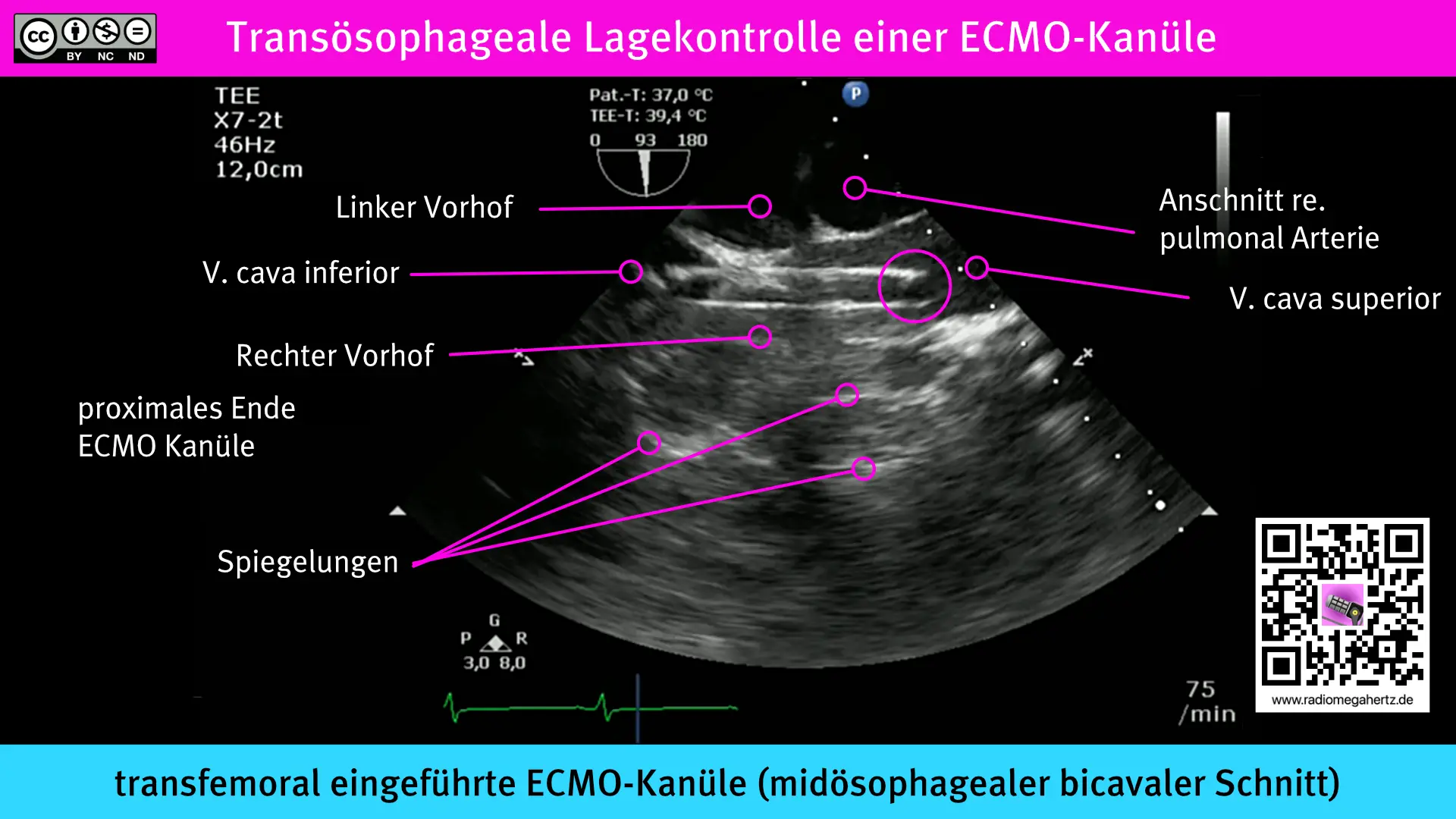
Mittels transösophagealer Echokardiografie (TEE) kann die korrekte Position, der über die Vena femoralis eingebrachten ECMO-Kanüle, kontrolliert werden. Vorzugsweise findet diese Prozedur während der Anlage statt. Die korrekte Lage der Spitze der drainierenden Kanüle wäre der Übergang der Vena cava inferior in den rechten Vorhof. Anhand des TEEs kann die Position der schallreflektierenden Kanülen sehr gut beurteilt und auch eine Lagekorrektur live mitverfolgt werden.
Die folgende Abbildung zeigt die venöse ECMO-Kanüle bis in die V. cava superior reichend und wurde entsprechend etwas zurückgezogen bis das Ende im rechten Vorhof lag.
Transthorakale Echokardiografie
Der retrograde Blutfluß in die A. thoracica bei Anlage einer V-A ECMO führt durch den Anstieg des arteriellen Mitteldrucks unvermeidbar zu einer Nachlasterhöhung für den linken Ventrikel.
Bei stark eingeschränkter Pumpfunktion kann dadurch eine Situation entstehen, in der das Herz zusätzlich belastet wird und dilatiert. Es könnte nicht mehr in der Lage sein, Blut über die Aortenklappe in die Aorta ascendens auszuwerfen.
Bei nicht öffnender Aortenklappe und stark gefülltem linken Ventrikel kann es durch die Stase des Blutes zur Thrombusbildung im linken Ventrikel kommen, was wiederum therapielimitierend werden kann. Post interventionem bietet die transthorakale Echokardiografie (TTE) in den typischen Standardschnitten daher eine weitere wichtige Option, die Herzfunktion beurteilen zu können.
Antegrade Perfusion
Das Größenverhältnis von nativem Gefäß und der erforderlichen ECMO-Kanüle kann so ungünstig sein, dass es zu einer Minderperfusion oder Ischämie der kanülierten Extremität kommen kann.
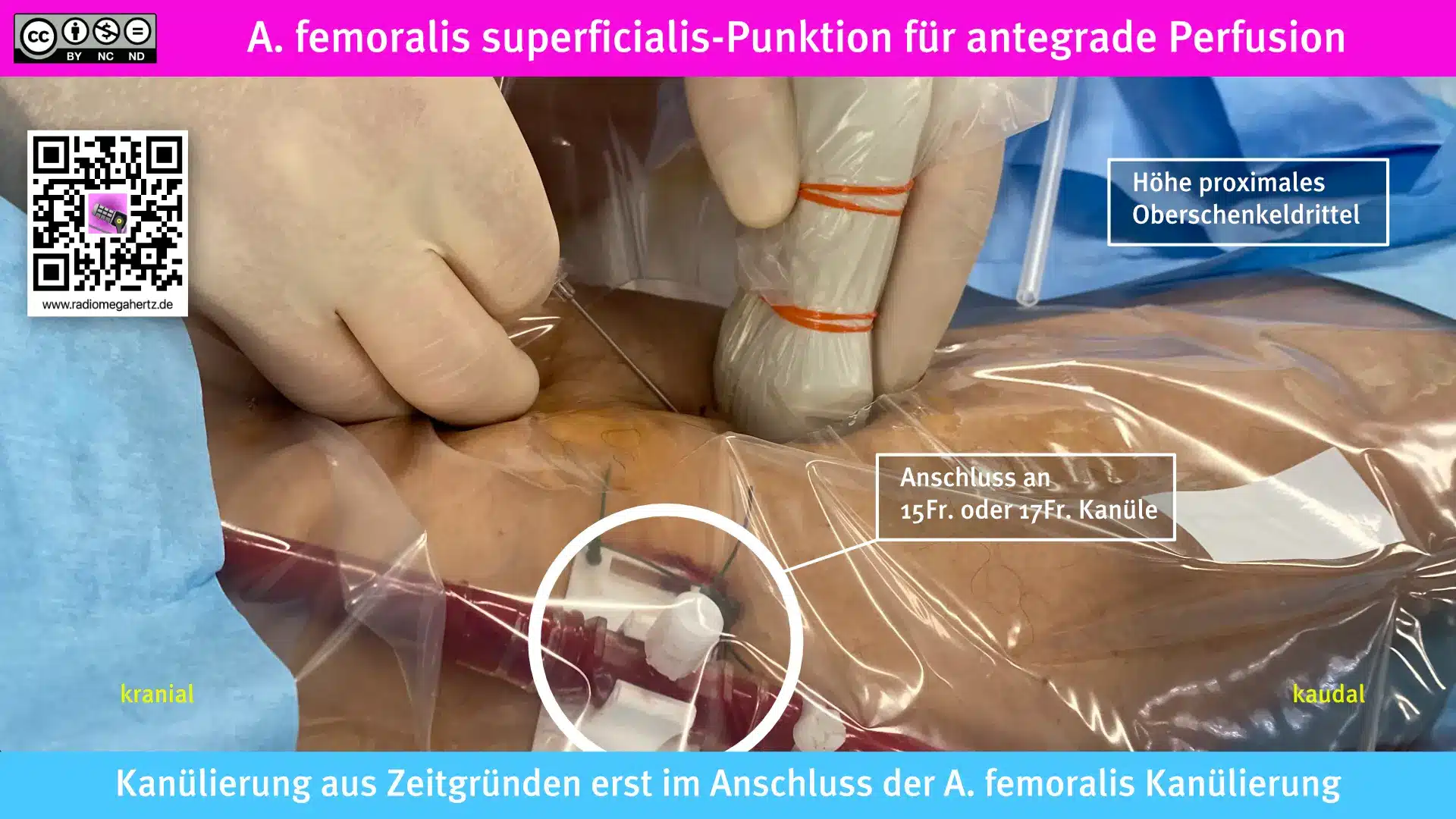
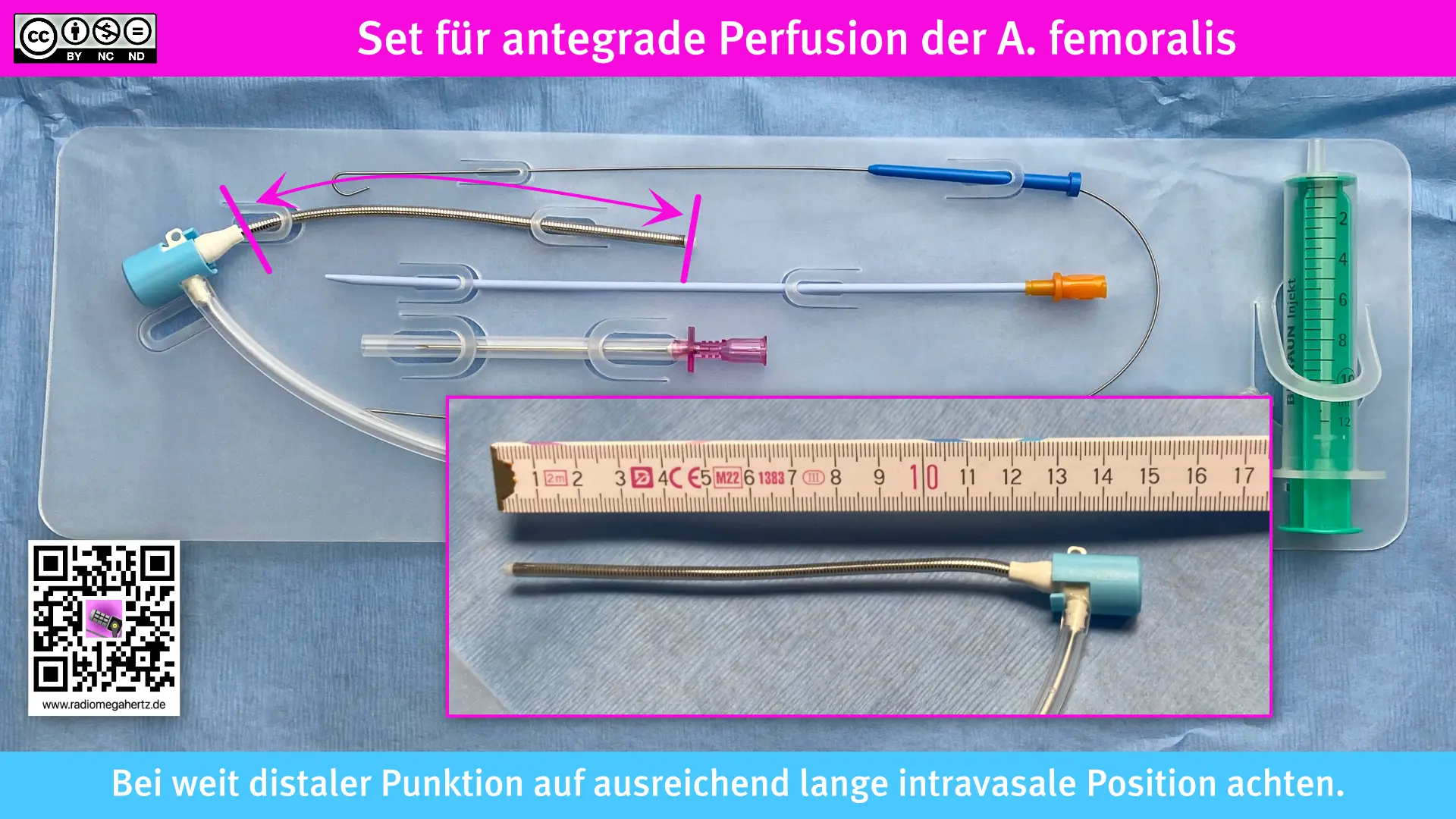
Wird diese Perfusionsstörung erkannt, z.B. durch NIRS–Sauerstoffsättigungsmessung in der Extremität, muss zeitnah eine zusätzliche Perfusionskanüle in Richtung der distalen Extremität gelegt werden. Das nennt man antegrade Perfusion. Über diese Kanüle kann dann oxygeniertes Blut aus der ECMO-Kanüle abgenommen und das Bein (oder der Arm) auch bei okkludiertem Nativgefäß ausreichend perfundiert werden. Auf diese Weise können Blutflüsse bis ca. 300 ml/min erreicht werden, die auch für größere Extremitäten ausreichend sind. Für die Anlage der distalen, antegraden Kanüle drängt sich der Einsatz der Sonografie natürlich auf.
Punktion der A. femoralis superficialis nach distal
Fehllagen können für Patient*innen desaströse Auswirkungen haben
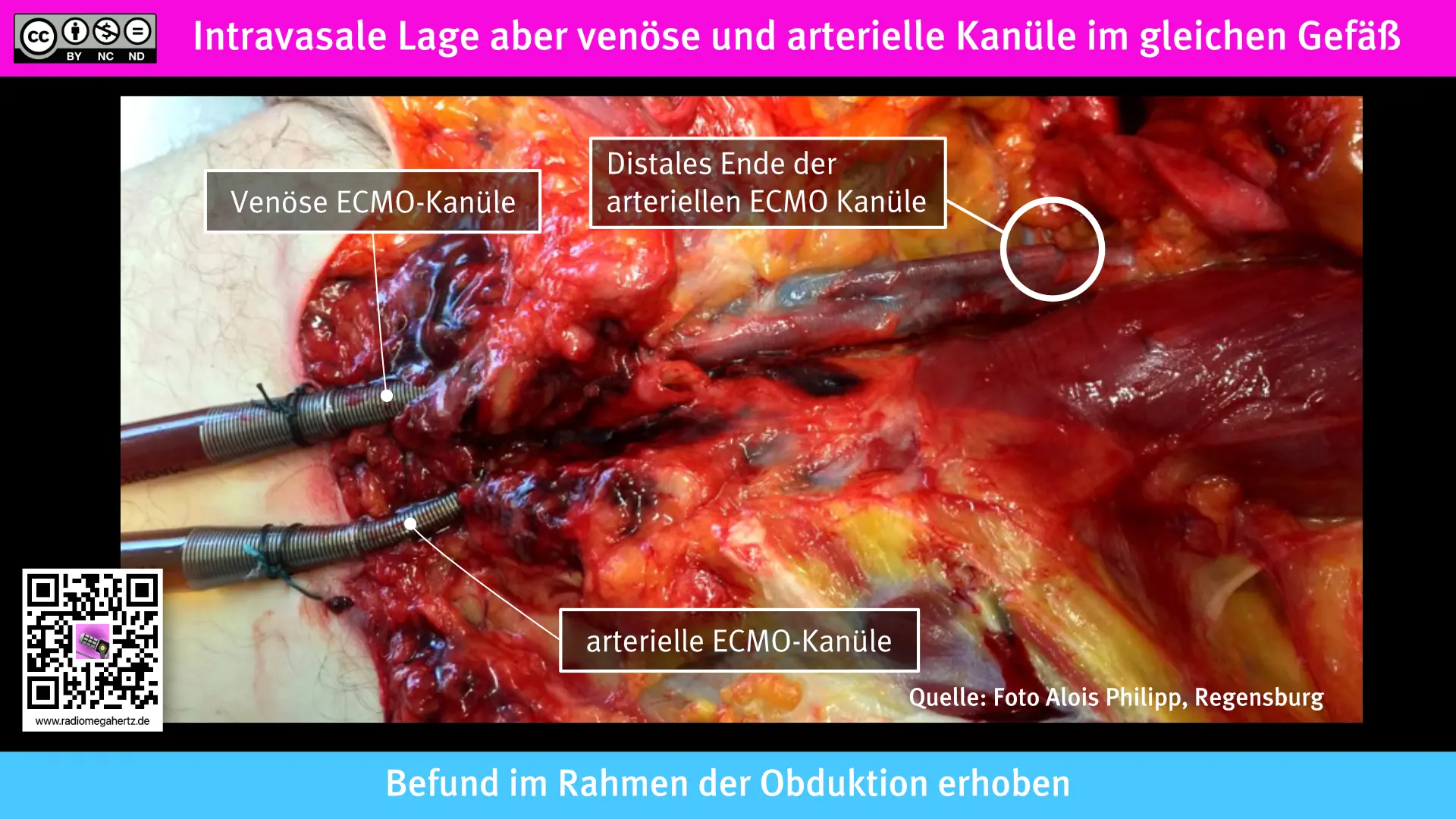
Glücklicherweise kommen so schwere Komplikationen, wie in den folgenden Abbildungen dargestellt, nicht häufig vor. Aber, es zeigt, wie invasiv die ECMO Kanülierung ist und bei Komplikationen den Tod von Patient*innen bedeuten kann.
In der folgenden Abbildung liegen die arterielle und venöse ECMO Kanüle gemeinsam in der V. femoralis. Die geplante V-A ECMO Anlage schlug fehl.
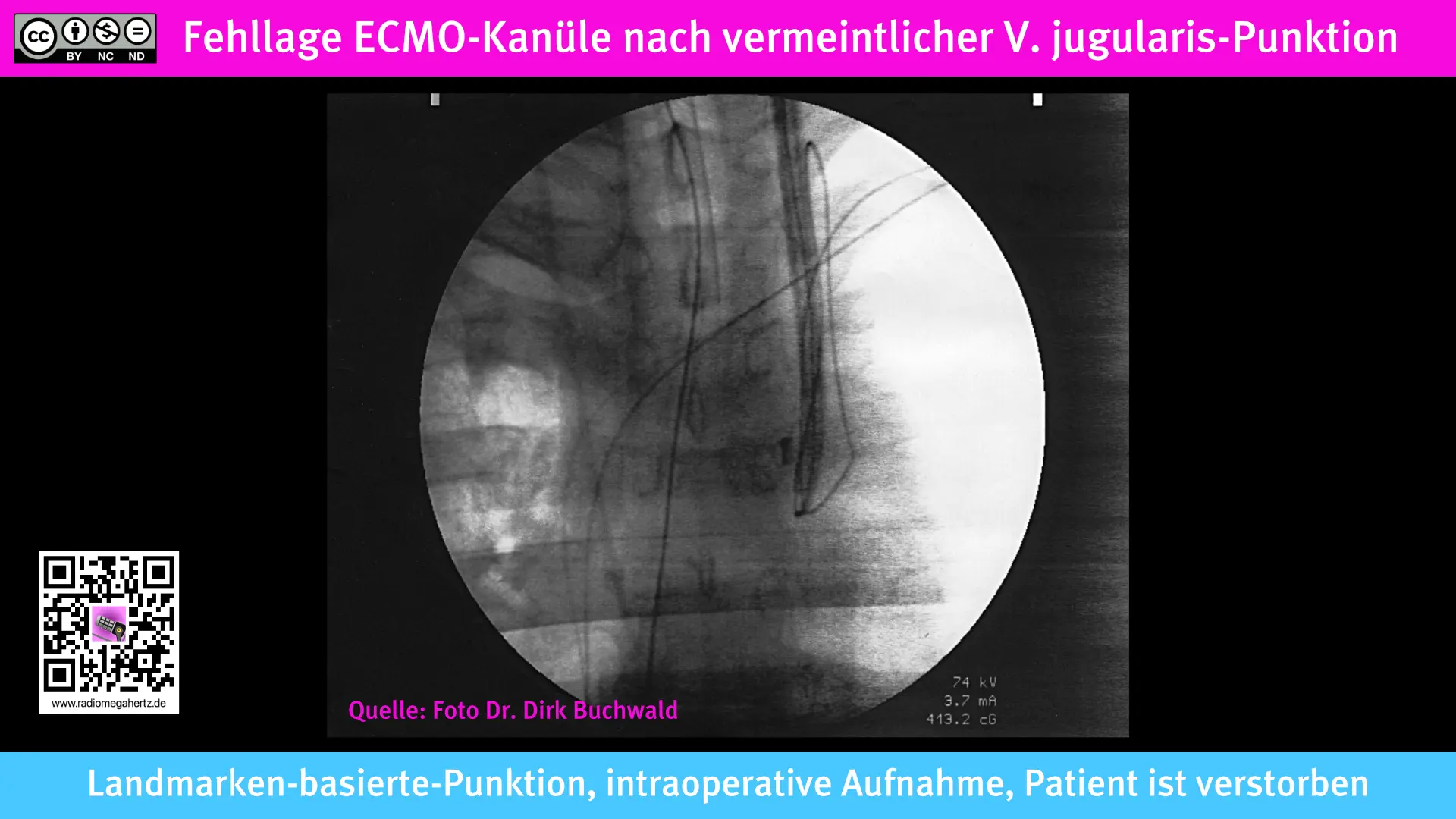
Extravasale, frei im Bauchraum liegende ECMO Kanülen. Radiologische Lagekontrolle beim Problemerkennung in der Phase des ECMO Anfahrens.
Versuch der linkseitigen venösen ECMO Kanülierung über die V. jugularis interna. Die Fotoaufnahme vom Röntgengerät ist schon mehrere Jahre alt.
ECMO-Themen, die nicht im Podcast besprochen wurden
A. axillaris Kanülierung: Pro und Kontra
Die A. axillaris / A. subclavia-Kanülierung ist eine Alternative zur A. femoralis-Punktion. Moussa et al. fanden in einer retrospektiven Studie bei über 372 Patient*innen im kardiogenen Schock und mit Anlage einer VA-ECMO keine Vorteile für die A. axillaris / A. sublcavia gegenüber der A. femoralis:
- Höhere Dislokationsrate
- vermehrt schwere Blutungen
- kein Vorteil bzgl. LV-Erholung (Nachlast) oder niedrigerer Lungenödemrate
- kein Unterschied in der 28-Tage-Mortalität
- kein Unterschied in der Erholung von der kardialen Grunderkrankung
Referenzen und Links
- Haas, A.; Busjahn, C.; Crede, D.; Kilger, E.; Reuter, D.A. [Extracorporeal membrane oxygenation and hemodynamics : Therapy is not only a friend of the heart]. Anaesthesiologie 2022, 71, 967–982. doi:10.1007/s00101-022-01230-8
Anmerkung: aus meiner Sicht ein absolut lesenswerter Artikel zur Indikation und Problematik mit ECMO-Therapien. Cheney, A.E.; McCabe, J.M. Alternative Percutaneous Access for Large Bore Devices. Circ Cardiovasc Interv 2019, 12, e007707. doi:10.1161/CIRCINTERVENTIONS.118.007707
Anmerkung: Inhalte zur A. axillaris Punktion und transcavalen Zugang.
Sandoval, Y.; Burke, M.N.; Lobo, A.S.; Lips, D.L.; Seto, A.H.; Chavez, I.; Sorajja, P.; Abu-Fadel, M.S.; Wang, Y.; Poulouse, A.; Gössl, M.; Mooney, M.; Traverse, J.; Tierney, D.; Brilakis, E.S. Contemporary Arterial Access in the Cardiac Catheterization Laboratory. JACC Cardiovasc Interv 2017, 10, 2233–2241. doi:10.1016/j.jcin.2017.08.058
Kaki, A.; Blank, N.; Alraies, M.C.; Kajy, M.; Grines, C.L.; Hasan, R.; Htun, W.W.; Glazier, J.; Mohamad, T.; Elder, M.; Schreiber, T. Access and closure management of large bore femoral arterial access. J Interv Cardiol 2018, 31, 969–977. doi:10.1111/joic.12571
Blakeslee-Carter, J.; Shao, C.; LaGrone, R.; Gonzalez-Sigler, I.; Sutzko, D.C.; Pearce, B.; Eudailey, K.; Spangler, E.; Beck, A.W.; McFarland, G.E. Vascular complications based on mode of extracorporeal membrane oxygenation. J Vasc Surg 2022, 75, 2037–2046.e2. doi:10.1016/j.jvs.2022.01.078
Moussa, M.D.; Rousse, N.; Abou Arab, O.; Lamer, A.; Gantois, G.; Soquet, J.; Liu, V.; Mugnier, A.; Duburcq, T.; Petitgand, V.; Foulon, V.; Dumontet, J.; Deblauwe, D.; Juthier, F.; Desbordes, J.; Loobuyck, V.; Labreuche, J.; Robin, E.; Vincentelli, A. Subclavian versus femoral arterial cannulations during extracorporeal membrane oxygenation: A propensity-matched comparison. J Heart Lung Transplant 2022, 41, 608–618. doi:10.1016/j.healun.2022.01.007
Deutsche Gesellschaft für Thorax- Herz- und Gefäßchirurgie e.V. (DGTHG). Federführende Fachgesellschaft. (2020). S3-Leitlinie Invasive Beatmung und Einsatz extrakorporaler Verfahren bei akuter respiratorischer Insuffizienz. Retrieved from https://register.awmf.org/de/leitlinien/detail/011-021
Rupprecht L, Lunz D, Philipp A et al. Pitfalls in percutaneous ECMO cannulation. Heart Lung Vessel. 2015(7):320-326.
Wang L, Yang F, Zhang S et al. Percutaneous versus surgical cannulation for femoro-femoral VA-ECMO in patients with cardiogenic shock: Results from the Extracorporeal Life Support Organization Registry. J Heart Lung Transplant. 2022(41):470-481.
Feedback zum Beitrag
Hat die der Beitrag gefallen? Wenn ja, freue ich mich über eine Rückmeldung. Wenn nicht, schreibe mir doch warum. Email an: support@radiomegahertz.de.